商机详情 -
黑龙江近红外二区X射线-荧光双模态成像系统常用知识
双模态数据的病理关联分析:影像与组织学的定量整合系统支持双模态影像与组织病理学数据的配准分析,在骨**研究中,将X射线的骨破坏区域、荧光的肿瘤细胞分布与病理切片的HE染色结果叠加,可量化影像指标与病理分级的一致性(如G3级**的荧光强度较G1级高3倍)。这种整合分析使影像诊断的准确率从75%提升至92%,并能发现传统病理难以量化的空间分布特征,如肿瘤细胞沿骨小梁间隙的浸润模式。 X射线—荧光双模态成像系统支持骨靶向纳米药物的分布评估,X射线定位骨骼,荧光追踪药物蓄积。X射线—荧光双模态成像系统的三维重建功能,构建骨骼—肿块的立体关联模型。黑龙江近红外二区X射线-荧光双模态成像系统常用知识
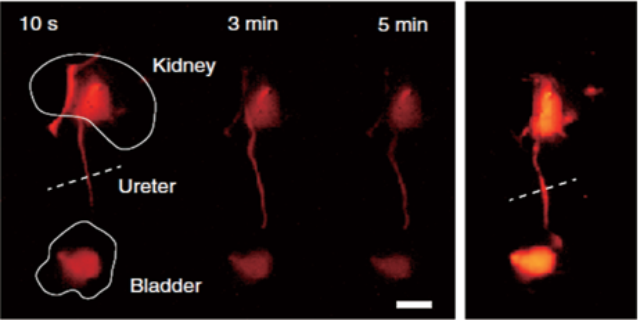
自适应剂量调节:辐射安全与成像效率的平衡双模态系统的智能剂量算法可根据样本厚度自动调节X射线参数(10-50kV),在小鼠全身骨成像中将单次辐射剂量控制在0.5mGy以下(相当于胸部CT的1/10),同时通过近红外二区荧光(1000-1700nm)提升分子信号的信噪比(达8:1)。在长期纵向研究中,该技术可实现每周2次的重复扫描,追踪骨转移*的进展与***响应,较传统高剂量X射线方案减少动物辐射损伤风险达70%。双模态系统的辐射防护铅舱设计,将操作人员暴露剂量控制在安全阈值以下。中国澳门X射线-荧光双模态成像系统推荐货源低剂量X射线扫描(<1mGy)与高灵敏度荧光检测结合,实现长期纵向的骨骼分子成像。

术中放疗剂量引导:双模态影像的医治优化结合X射线的骨结构成像与荧光标记的放疗敏感器(如H2AX探针),系统在骨肿块术中放疗中实时评估剂量分布:X射线定位肿块边界,荧光监测放疗诱导的DNA损伤(荧光强度与剂量呈线性相关,R²=0.98)。该技术可避免传统放疗的剂量盲区,在犬骨肿块模型中使肿块局部控制率提升30%,同时通过荧光信号调控放疗剂量,将正常骨组织的辐射损伤降低50%,实现“精细放疗-保护正常组织”的双重目标。该系统在骨代谢疾病中通过X射线评估骨转换率,荧光标记代谢相关蛋白酶活性。
双模态成像的辐射防护创新:操作人员安全保障系统采用磁屏蔽铅舱设计(铅当量1.5mm),配合自动曝光控制技术,将操作人员的辐射暴露剂量控制在0.1mSv/小时以下(相当于天然本底辐射的1/10)。同时,荧光模块的近红外光源(1064nm)功率<10mW/mm²,避免对实验动物和操作人员的光损伤。这种安全设计使系统符合实验室辐射安全标准,支持长时间连续成像实验,如24小时动态追踪骨折愈合的早期炎症反应。该系统在骨再生医学中通过X射线监测植入物骨整合,荧光标记干细胞分化轨迹。轻量化设计的双模态探头适用于小动物骨科模型,如小鼠股骨骨折的纵向双模态监测。

骨免疫学研究:微环境与结构的关联解析结合X射线的骨结构分析与荧光标记的免疫细胞(如CD45+白细胞),系统在骨髓炎模型中观察到炎症细胞聚集区域(荧光强度高2.5倍)的骨小梁破坏程度较非聚集区严重3倍,且通过时序成像发现免疫细胞浸润先于骨破坏24小时。这种“免疫-骨”互作的可视化技术,为骨免疫学研究提供空间与时间维度的动态数据,助力开发靶向骨微环境的免疫医治策略。在骨肿块药敏实验中,X射线—荧光成像系统量化肿块体积变化与荧光标记的细胞凋亡信号。该系统在骨科植入物研究中通过X射线评估材料骨结合,荧光标记周围组织炎症反应。中国澳门X射线-荧光双模态成像系统推荐货源
高灵敏度荧光探测器与微焦斑X射线源集成,使系统实现骨微结构与分子信号的双重解析。黑龙江近红外二区X射线-荧光双模态成像系统常用知识
X射线—荧光双模态成像系统:骨骼与分子的精细对话该系统创新性融合X射线的高分辨率解剖成像(5μm微焦斑)与近红外荧光的分子标记能力,在骨肿块研究中可同步呈现溶骨***灶的X射线灰度变化(骨皮质破坏程度)与荧光探针标记的肿瘤细胞活性(如Ki67蛋白表达)。通过智能配准算法,自动将X射线骨结构与荧光信号叠加,形成“解剖-分子”关联图谱,例如在小鼠股骨肿块模型中,可量化肿块体积与荧光强度的相关性(R²=0.91),较单一模态更精细评估肿块进展。黑龙江近红外二区X射线-荧光双模态成像系统常用知识