商机详情 -
黑龙江小动物X射线-荧光双模态成像系统采购信息
双模态成像的药物代谢动力学研究:骨骼靶向药物的时空分布通过X射线定位骨骼身体部位,荧光标记药物分子(如1100nm标记的唑来膦酸),系统可追踪药物从血液循环到骨表面的动态过程:静脉注射后5分钟药物在骨髓腔分布,2小时浓集于骨小梁表面,24小时达峰值(骨/血浆浓度比15:1)。结合X射线的骨密度分区(如松质骨vs皮质骨),可量化药物在不同骨区域的蓄积差异(松质骨蓄积量较皮质骨高3倍),为骨骼药物的剂型设计与给药物方案案优化提供时空分布数据。X射线—荧光双模态成像系统的AI模型预测功能,基于双模态数据预测骨肿块的转移风险。黑龙江小动物X射线-荧光双模态成像系统采购信息

轻量化便携设计:床边与术中的灵活应用针对临床转化需求,双模态系统开发了便携式版本(主机重量<10kg),X射线模块采用平板探测器(10×10cm),荧光通道集成光纤阵列探头,可在动物手术室或病床边实现即时成像。在骨科急症中,该设备可快速评估骨折类型(X射线)与周围组织损伤(荧光标记的炎症因子),为急诊手术方案提供影像支持,从成像到报告的全流程耗时<15分钟,较传统影像学检查效率提升50%。该系统在骨发育研究中通过X射线追踪骨骼生长板变化,荧光标记生长因子表达动态。陕西X射线-荧光双模态成像系统生产过程X射线—荧光双模态成像系统的骨微CT与荧光显微的联合成像,解析骨小梁微结构与细胞分子互作。
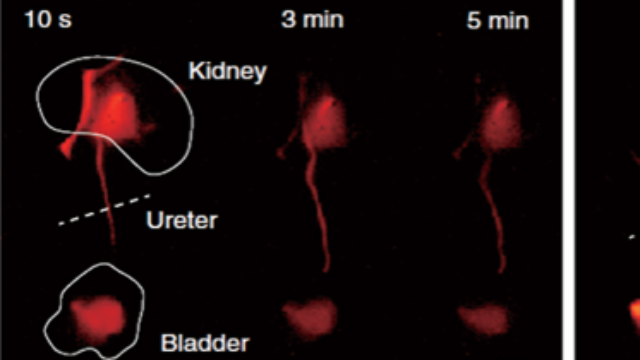
手术导航与术后评估:全流程诊疗支持双模态系统贯穿骨肿块诊疗全周期:术前通过X射线-荧光成像制定切除范围(如肿块边界外5mm),术中实时导航确保切缘阴性,术后通过双模态复查评估骨愈合(X射线骨痂密度)与肿瘤复发(荧光标记残留细胞)。在兔胫骨肿块模型中,该全流程方案使肿块局部控制率达90%,且术后6周的骨愈合评分(X射线骨密度+荧光血管密度)较传统手术提升40%,展现“诊断-医治-评估”的一体化优势。 磁兼容设计的双模态系统可与MRI设备联动,补充软组织信息与骨骼分子成像数据。
骨科生物材料研发:双模态评估的全周期支持在骨替代材料研发中,系统通过X射线监测材料降解速率(密度下降率)与新骨形成效率(骨体积增加),荧光标记材料周围的免疫细胞与血管内皮细胞,评估生物相容性与血管化程度。在β-TCP陶瓷研究中,双模态成像显示材料6周降解率达30%,伴随新骨体积增加25%,且荧光标记的CD68+巨噬细胞数量逐渐减少,为材料优化提供“降解-成骨-免疫”的多维度数据,加速研发进程。在骨扩散研究中,X射线—荧光成像系统识别骨皮质破坏,荧光标记细菌生物膜分布。动态时序采集功能让X射线—荧光成像系统记录骨折修复中骨痂矿化与血管生成的时空关联。
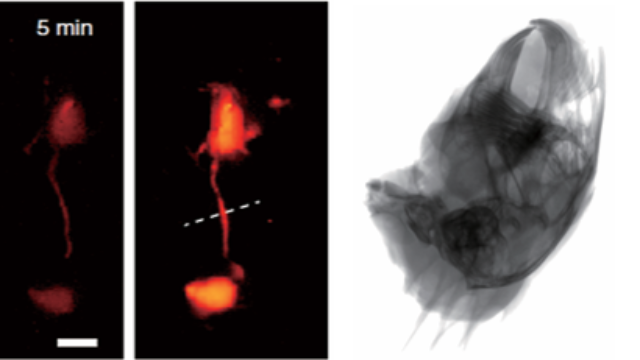
双模态成像的未来技术升级:AI+多模态的智能融合系统预留AI算法接口与多模态扩展端口,未来可集成机器学习模型(如基于Transformer的骨疾病预测网络)与质谱成像(MALDI),实现“X射线结构-AI预测-荧光验证-质谱代谢”的四维分析。在概念验证实验中,AI模型基于双模态数据预测骨肿块的转移风险(AUC=0.95),并通过质谱成像验证预测区域的代谢异常(如脂质代谢通路打开),为骨骼疾病的精细医学研究开辟“影像-分子-代谢”的多维研究范式。该系统在骨关节炎研究中通过X射线评估软骨下骨变化,荧光标记炎症因子表达。江西荧光X射线-荧光双模态成像系统推荐货源
实时影像融合技术让双模态系统在骨科手术中同步显示X射线骨解剖与荧光标记的肿块边缘。黑龙江小动物X射线-荧光双模态成像系统采购信息
X射线—荧光双模态成像系统:骨骼与分子的精细对话该系统创新性融合X射线的高分辨率解剖成像(5μm微焦斑)与近红外荧光的分子标记能力,在骨肿块研究中可同步呈现溶骨***灶的X射线灰度变化(骨皮质破坏程度)与荧光探针标记的肿瘤细胞活性(如Ki67蛋白表达)。通过智能配准算法,自动将X射线骨结构与荧光信号叠加,形成“解剖-分子”关联图谱,例如在小鼠股骨肿块模型中,可量化肿块体积与荧光强度的相关性(R²=0.91),较单一模态更精细评估肿块进展。黑龙江小动物X射线-荧光双模态成像系统采购信息